99、丙酸血症
罕见病诊疗指南2019年版
【概述】丙酸血症(propionic acidemia,PA) 又称丙酰辅酶 A 羧化酶缺乏症(Propionyl- CoA carboxylase deficiency)、酮症性高甘氨酸血症(Ketotic hyperglycinemia) 或丙酸尿症(Propionic aciduria),是一种常染色体隐性遗传的有机酸血症。PA 由编码线粒体多聚体酶丙酰辅酶 A 羧化酶(PCC) 基因 PCCA 或 PCCB 缺陷所致。PCC 缺乏可导致体内丙酰辅酶A 转化为甲基丙二酰辅酶 A 异常、丙酸及其相关代谢物异常蓄积,导致有机酸血症,并造成一系列生化异常、神经系统和其他脏器损害症状。
病因和流行病学
PA 致病基因分别为 PCCA 和 PCCB。PCCA 位于 13q32,含 24 个外显子,编码 728 个氨基酸,已报道突变124 种。PCCB 位于3q21-q22,包含15 个外显子,编码539 个氨基酸, 已报道突变 114 种(http://www.hgmd.cf.ac.uk)。PCCA 或 PCCB 突变使丙酰辅酶 A 羧化酶缺乏,导致丙酰辅酶 A 转化为甲基丙二酰辅酶 A 受阻,进而引起体内丙酸及其前体丙酰CoA、甲基枸橼酸和丙酰甘氨酸等代谢产物异常增高,引起机体损伤。
PA 总患病率在国外不同人种之间为 1/100 000~100/100 000, 我国为 0.6/100 000~ 0.7/100 000。
临床表现
主要为高血氨、脑损伤和心肌病等。
1. 新生儿起病型 出生时正常,开始哺乳后出现呕吐、嗜睡、肌张力低下、惊厥、呼吸困难、高血氨、酮症、低血糖、酸中毒、扩张型心肌病、胰腺炎等异常,病死率高。
2. 迟发型 常因发热、饥饿、高蛋白饮食和感染等诱发,表现为婴幼儿期喂养困难、发育落后、惊厥、肌张力低下等。由于丙酸等有机酸蓄积,许多患者的认知能力及神经系统发育受到损害,脑电图慢波增多或见癫痫波;一些患者可有骨折,X 线见骨质疏松;还常造成骨髓抑制,引起粒细胞减少、贫血、血小板减少。也可有心脏损害,如心肌病、心律失常、QT 间期延长、心功能减弱等。肾功能损害较为少见。
辅助检查
1. 实验室常规检查 血常规示粒细胞减少或血三系减低,尿酮体阳性,血气分析可见酸中毒,血生化检查可见高血氨、高乳酸、低血糖和心肌酶升高等。
2. 血氨基酸和酯酰肉碱谱分析 甘氨酸水平增高,丙酰肉碱(C3)、丙酰肉碱 / 乙酰肉碱比值(C3/C2) 增高。
3. 尿有机酸分析 3- 羟基丙酸和甲基枸橼酸增高高度提示此病。
4. 头部 MRI/CT 可表现为脑萎缩、脑室增宽及基底节区异常信号。
5. 基因诊断 PCCA 或 PCCB 检出 2 个等位基因致病突变有确诊意义。
诊断
新生儿生后数小时到 1 周内出现拒乳、呕吐、嗜睡、肌张力低下、惊厥、呼吸困难、高血氨、酮症、低血糖、酸中毒等异常;婴幼儿不明原因反复呕吐、惊厥、意识障碍,严重的酸中毒、高血氨,伴有特殊的影像学异常及血液系统损害者,特别是有类似 / 不明原因死亡家族史时,应考虑到本病。进一步行血氨基酸和酯酰肉碱谱分析示甘氨酸水平增高,C3/C2 增高;尿有机酸分析见 3- 羟基丙酸和甲基枸橼酸增高,可临床诊断丙酸血症。确诊有赖于PCCA 或 PCCB 基因突变分析,检出 2 个等位基因致病突变有确诊意义。
鉴别诊断
1. 甲基丙二酸血症 该病患者也有血中丙酰肉碱、丙酰肉碱与游离肉碱比值增高, 但同时伴有尿液中的甲基丙二酸、甲基枸橼酸异常增加,而 PA 患者尿中的甲基丙二酸水平正常。
2. 多种羧化酶缺乏症(包括生物素酶缺乏症、全羧化酶合成酶缺乏症) 患者尿中的3- 羟基丙酸、甲基巴豆酰甘氨酸及丙酰甘氨酸增高,与 PA 类似;但血酰基肉碱谱的 3- 羟基异戊酰肉碱增高,而 PA 患者的该指标正常。
3. 糖尿病酮症酸中毒、乳酸性酸中毒或其他有机酸血症等可通过血尿代谢物的质谱分析鉴别诊断。
治疗
1. 急性期治疗 以补液,纠正酸中毒、低血糖和电解质紊乱为主,同时限制天然蛋白质摄入,供给足量热量。可予静脉滴注左卡尼汀促进酸性物质的代谢和排出。如出现高氨血症,可予精氨酸静脉滴注,口服促肠蠕动剂、氨甲酰谷氨酸等。若高氨血症或代谢性酸中毒难以控制时,还需通过腹膜透析或血液透析去除毒性代谢物。
2. 长期治疗
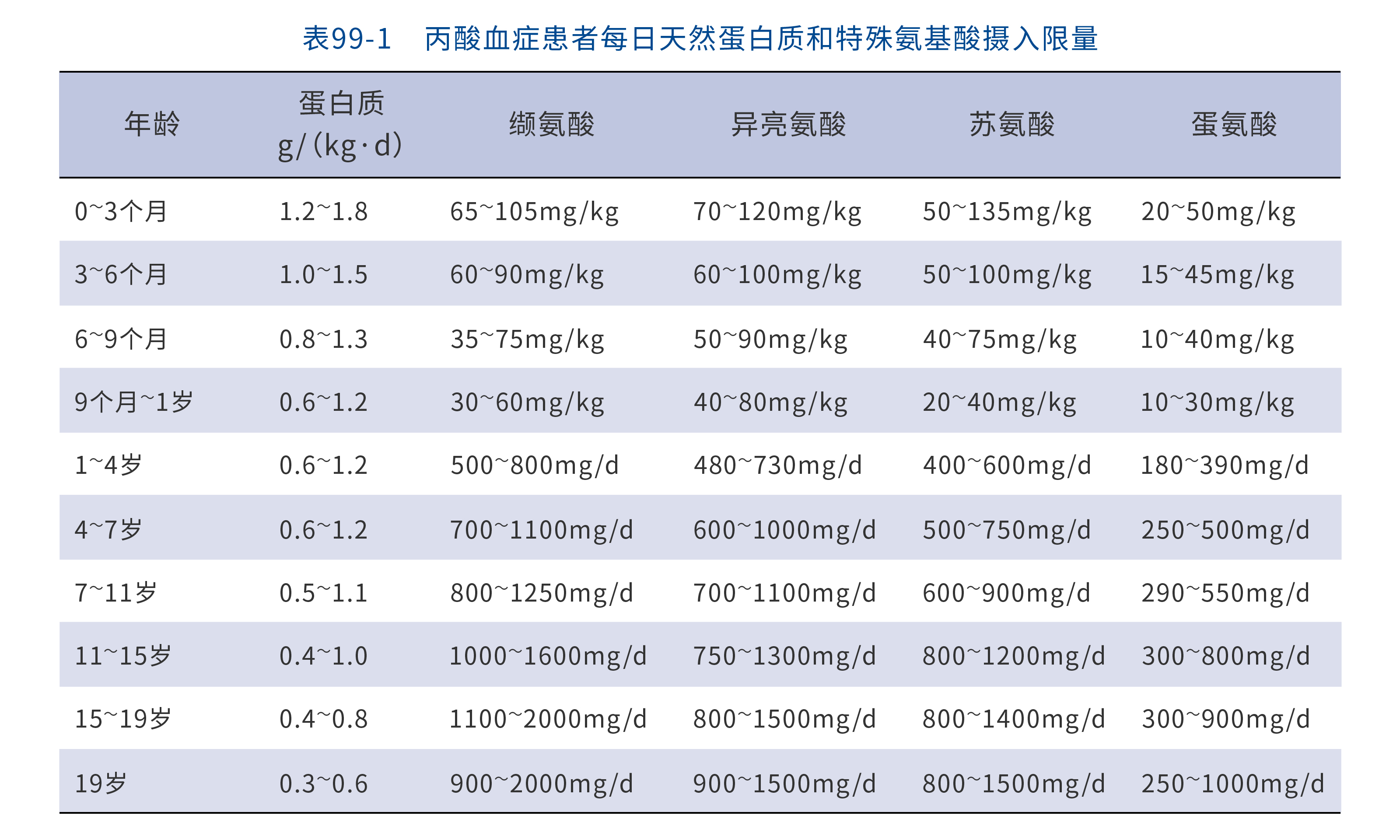
(1) 饮食控制:PA 患者应以限制天然蛋白质膳食为主,但要保证足够的蛋白质和能量摄入。推荐以不含缬氨酸、异亮氨酸、苏氨酸、蛋氨酸的特殊配方营养粉喂养,以减少丙酸的产生,并可改善患儿的发育和营养状态;但因这些氨基酸为必需氨基酸,故特殊配方奶粉不能作为蛋白质的唯一来源,还应进食少量天然蛋白质。每日所需总蛋白质的量, 婴儿为 8~12g,儿童为 30~40g,成人为 50~65g,天然蛋白质和几种特殊氨基酸的限量见表99-1,不足部分以不含缬氨酸、异亮氨酸、苏氨酸和甲硫氨酸的配方奶或蛋白质替代。临床上通常从特殊奶粉与天然蛋白质 1 :3 配比开始,再根据血氨基酸水平及代谢物浓度调整二者的比例,以达到有效控制代谢异常。同时避免饥饿,抑制肌肉组织和脂肪组织分解代谢。
由于长期限制天然蛋白质,PA 患者易发生微量营养素和矿物质(维生素 B12、维生素A、维生素 D、叶酸、钙、锌) 缺乏,需注意监测,必要时相应补充。
(2) 药物治疗
1)左卡尼汀:PA 患者常合并继发性肉碱缺乏,左卡尼汀可与有机酸结合,形成水溶性代谢物,从尿液排出体外,促进有机酸的排泄,因此急性期需静脉滴注左卡尼汀[50~100mg/(kg·d)] 。部分患儿用药后可能出现轻度腹泻,无须特殊处理。
2)新霉素或甲硝唑:可被用于抑制肠道细菌,通过减少肠道细菌代谢而减少丙酸的产生。PA 患者可在急性期口服新霉素 50mg/(kg·d),甲硝唑 10~20mg/(kg·d)。因长期应用抗生素可能导致肠道内菌群紊乱,不建议长期用药。
3)氨甲酰谷氨酸:如 PA 患者存在明显的高氨血症(如血氨 >400μmol/L),可考虑应用氨甲酰谷氨酸进行治疗。它在 PA 急性失代偿期对高血氨有解毒作用,可通过有效降低血氨水平,减少尿丙酰甘氨酸的排泄,增加游离肉碱和总肉碱水平,从而改善 PA 患者的代谢稳定性。起始剂量为 100~250mg/(kg·d),分 2~4 次给药。
(3) 肝移植:对少数经过良好膳食控制仍频繁发生严重代谢失代偿、既往有同胞死亡或有心肌病的 PA 患者,可考虑进行肝移植。据报道,肝移植后一些患者临床症状明显改善,无须进行饮食限制和其他医学治疗,一些病变如心肌病等也是可逆的。作为原位肝移植的方法之一,也可考虑辅助性原位肝移植,可保留患儿的部分肝脏,以便将来进行基因治疗,并且还可以为移植失败的病例提供暂时性功能支持。据报道,1 例接受辅助性原位肝移植的 PA 患者,随访 10 年内未进行饮食控制和药物治疗,临床和生化指标正常,精神运动发育和智力水平接近正常。由于多数 PA 患者伴有严重的脑损伤,肝移植应在早期且在患儿身高 >-2SD 时进行,以便提升效果,改善预后。
3.遗传咨询 丙酸血症是常染色体隐性遗传病,患者父母再次生育再发风险为 25%。应对所有患者及其家庭成员提供必要的遗传咨询,对高风险胎儿进行产前诊断。
诊疗流程
.png)
作者
北京协和医院儿科 孙之星 邱正庆
参考文献
[1] BaumgartnerMR,H rsterF,Dionisi-Vici C,et al.Proposed guidelines for the diagnosis and management of
methylmalonic and propionic acidemia.Orphanet J Rare Dis,2014,9 :130.
[2] Chapman KA,Gropman A,MacLeod E,et al.Acute management of propionic acidemia.Mol Genet Metab, 2012,105 :16-25.
[3] 韩连书,胡宇慧 . 丙酸血症发病机制及诊治研究进展 . 实用儿科临床杂志,2008,23(20):1561-1563.
[4] Rela M,Battula N,Madanur M,et al.Auxiliary liver transplantation for propionic acidemia:A 10-year follow- up.Am J Transplant,2007,7(9):2200-2203.
[5] http://www.ncbi.nlm.nih.gov/sites/genetests
更新时间
2019年11月


