研究前沿--CD19 CAR T细胞治疗难治性全身型重症肌无力的病例报告
罕见病联盟
编译:复旦大学附属华山医院神经内科 赵重波
《柳叶刀-神经学》2023年12月发表了一项病例研究,研究对象是一位33岁的女性,为乙酰胆碱受体抗体阳性的难治性全身性重症肌无力(MG),通过抗CD19嵌合抗原受体(CAR)T细胞疗法(CAR-T细胞)获得了有效的治疗。
该患者于2012年被诊断为MG,先后经历了包括胸腺切除术、乙酰胆碱酯酶抑制剂、糖皮质激素、B细胞消耗性抗体(利妥昔单抗)、蛋白酶体抑制剂(硼替佐米)、免疫抑制药物(吗替麦考酚酯)和免疫球蛋白等治疗。但病情依然不稳定,经历多次危象,需要重症监护和侵袭性气道管理。
鉴于其病情的难治性,医疗团队决定采用新型的CAR T细胞治疗方法:一种二代抗CD19 CAR T构建体(KYV-101,Kyverna Therapeutics,美国加州埃默里维尔),无明显细胞因子释放综合征和神经毒性报道。其构建体包括一个完全人源化的CD19结合域、一个CD8α铰链和跨膜域、一个CD28共刺激域和一个CD3ξ激活域。
- 全人源化CD19结合域:这是CAR T细胞识别和结合到B细胞表面CD19分子的部分,用于靶向含有CD19的B细胞。
- CD8α铰链和跨膜域:这部分使CAR T细胞能够稳定地表达在T细胞表面,并通过铰链区域提供一定的灵活性。
- CD28共刺激域:这是CAR T细胞激活过程中提供第二信号的部分,有助于T细胞的充分激活和功能。
- CD3ξ激活域:这是传递激活信号至T细胞内部的关键部分,促使T细胞进行增殖、分泌细胞因子和杀伤靶细胞。
在进行收集白细胞和CAR T细胞输注之前,患者糖皮质激素减至低剂量(10mg),同时吗替麦考酚酯恢复使用直到开始消耗淋巴细胞治疗前2天,收集白细胞后在体外成功制备CAR-T后进行扩增,消耗淋巴细胞的方案为氟达拉滨(30 mg/m²,治疗前第-6、-5和-4天)和环磷酰胺(300 mg/m²,治疗前第-6、-5和-4天),患者在耗竭淋巴细胞后接受一次剂量为1×10^8个CD19 CAR T细胞输注。
患者接受治疗后耐受性良好,没有与CAR T细胞治疗相关的不良事件,如细胞因子释放综合症、免疫效应细胞相关的神经毒性综合征、造血系统重建不足或低丙种球蛋白血症(IgG<5g/L)等。患者出现了转氨酶升高,但仅为轻度且呈自限性,未经治疗即自行缓解。
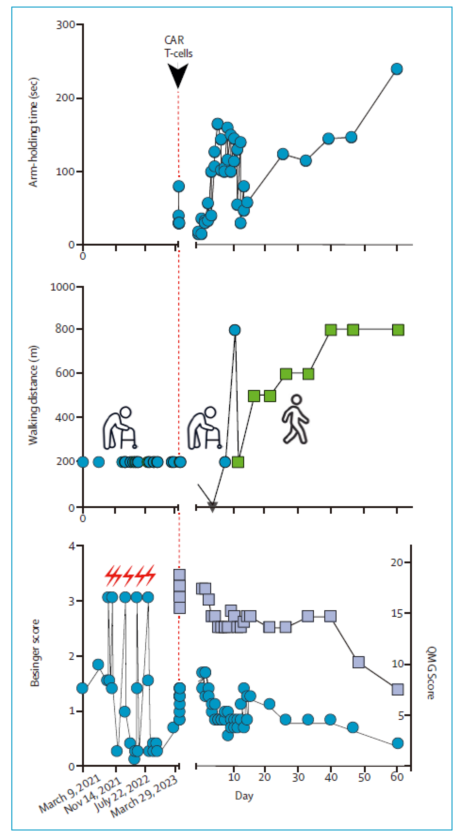
患者在接受CD19 CAR T细胞治疗后,第8天循环中CD19 B细胞被清除,在第62天也未检测到。抗-AchR抗体降低70%,但保护性疫苗的IgG滴度能得以保持。此后的2月内患者的肌肉力量和疲劳状况均得到改善,临床多参数Besinger疾病活动评分和量化重症肌无力QMG评分均有降低。CAR T细胞在第16天达到峰值扩张(每微升131个细胞;占总CD3 T细胞的16%),在第62天时仍然可以检测到(每微升0.5个细胞,占总CD3 T细胞的0.19%)。
本病例探索性治疗表明,CD19 CAR T细胞可能对基于自身反应性B细胞和自身抗体的多种自身免疫性疾病有效。作者强调了由于神经系统自身免疫病的严重性和目前有限的治疗选择,需要新的治疗方法。
然而,我们需要注意本文的局限性:①单一病例报告:研究讨论了对单一患者的治疗。虽然结果令人鼓舞,但在没有对更多患者群体进行进一步研究的情况下,这些结果不能被推广。②随访时间短:患者在治疗后被观察了62天。在这么短的时间内无法评估长期疗效和安全性。③缺乏对照组:没有对照组,很难确定观察到的效果是否完全归因于CAR T细胞治疗,或可能受到其他因素的影响。④之前的治疗:在接受CAR T细胞治疗之前,患者已经接受了多种治疗,这可能影响了疾病的进程或对新治疗的反应。⑤潜在的不良效应:虽然在这个案例中没有报告严重的不良事件,但CAR T细胞疗法已知可能引起严重的副作用,这些副作用可能在研究期间没有被观察到。⑥长期免疫力的随访:治疗对患者长期免疫力的影响,特别是保护性抗体的产生,没有得到充分探索。
为了充分解决这些局限性,需要进行更多具有更大样本量、对照组、更长随访时间和详细经济评估的研究。
参考文献(1)
1. Haghikia A, Hegelmaier T, Wolleschak D, Bottcher M, Desel C, Borie D, et al. Anti-CD19 CAR T cells for refractory myasthenia gravis. Lancet Neurol. 2023;22(12):1104-5.